Taula periòdica
150 ANYS DE LA TAULA PERIÒDICA
L’Assemblea General de les Nacions Unides, a través de la UNESCO, ha declarat 2019 com l’Any Internacional de la Taula Periòdica dels Elements Químics (IYPT2019) per tal de commemorar el 150é aniversari de la seua creació
A mitjans del segle XIX els químics coneixien 63 elements, però no es posaven d’acord en com ordenar-los. Per tal de trobar la manera de fer-ho i de discutir altres qüestions que els tenien dividits com la nomenclatura química i la distinció entre àtom i molècula entre d’altres, en 1860 es va realitzar el primer Congrés Internacional de Químics a Karlsruhe (Alemanya). Allí es va establir també el concepte de “pes atòmic”, actualment massa atòmica relativa d’un element.
Basant-se en aquest concepte Dimitri Mendeléiev (1834-1907) es va adonar d’un fet singular: si s’ordenaven els elements en funció del seu pes atòmic, s’observaven una sèrie de propietats que apareixien de manera periòdica al llarg de l’ordenació. Cada vegada que es repetia la propietat es començava una nova columna, configurant-se així una presentació en forma de taula. Aquests resultats es van presentar en 1869, fa exactament 150 anys.
En aquesta estructura de taula Mendeléiev va deixar alguns buits i va aventurar que els elements que els ocupaven encara no s’havien descobert. Fins i tot va predir les propietats d’aquests elements desconeguts. Per exemple, el buit adjacent a l’alumini havia de correspondre, segons ell, a un metall amb una massa atòmica de 68, un punt de fusió baix i una densitat de 6 g/cm3. Sis anys més tard es va descobrir el gal·li que té una massa atòmica de 69,7, es fon amb la calor de la mà i té una densitat de 5,9 g/cm3. El mateix va passar amb l’escandi, el germani i el tecneci que no es va descobrir fins 30 anys després de la seva mort.
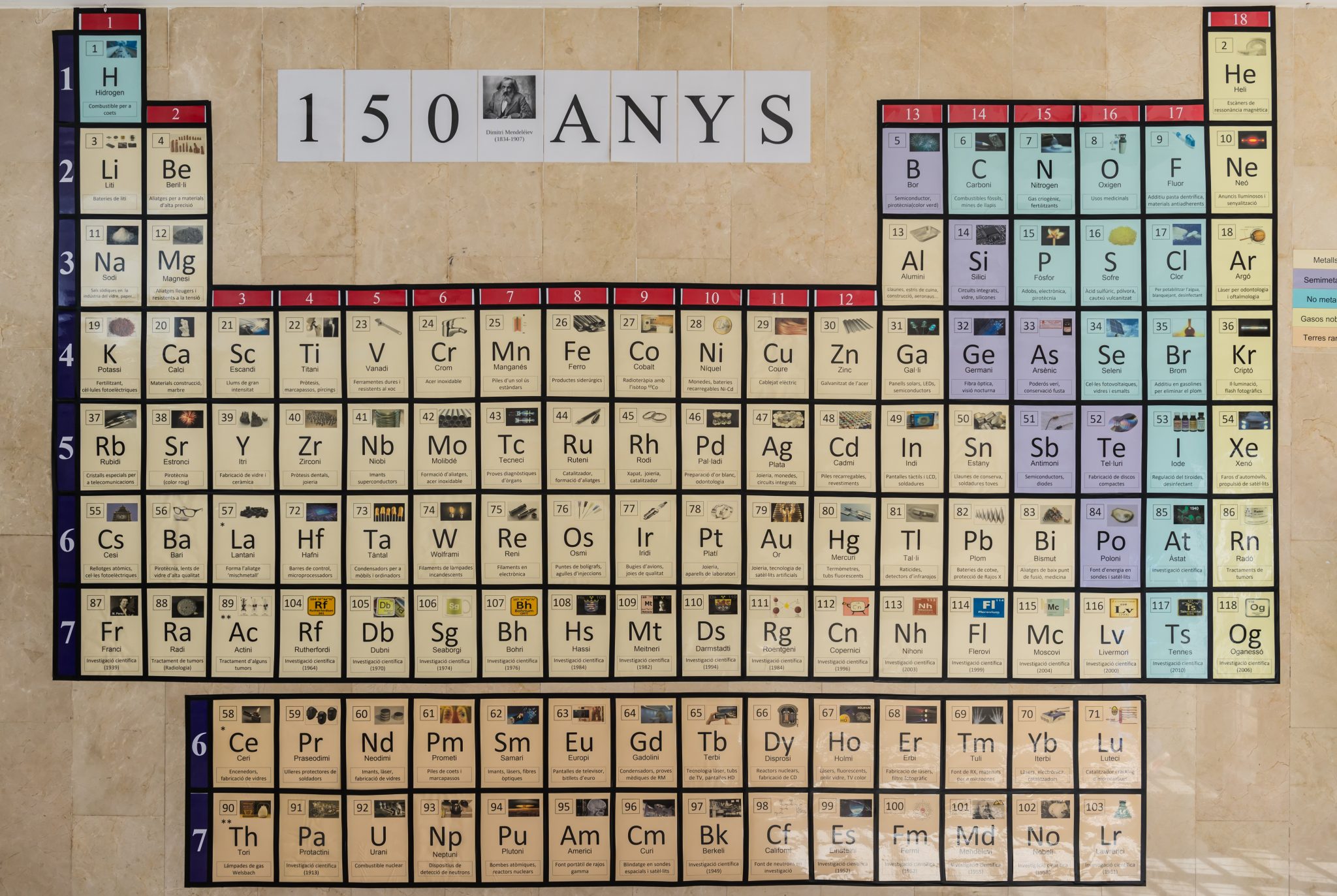
En la taula periòdica actual els elements es col·loquen d’esquerra a dreta i de dalt a baix en ordre creixent dels seus nombres atòmics (nombre de protons al nucli de l’àtom). Els elements estan ordenats en set fileres horitzontals anomenades períodes i divuit columnes verticals anomenades grups o famílies.
La grandesa de la taula periòdica està en la seua periodicitat, cada cert nombre de partícules subatòmiques que constitueixen els elements es repeteixen les propietats.
Al llarg dels anys s’han anat descobrint elements a la natura i se n’han fabricat d’altres en acceleradors de partícules. Avui dia hi figuren 118 elements, 55 més que en l’època de Mendeléiev. Els últims 28 elements descoberts s’han creat en explosions nuclears o en laboratoris i alguns d’ells tant sols han estat estables mil·lèsimes de segon. La pregunta que ens fem és: hi ha més elements que els 118 coneguts? Càlculs recents indiquen que en podrien ser 170, només cal estar atents als acceleradors de partícules en els propers anys.
Departament de FÍSICA I QUÍMICA


