
Las separación de mezclas por métodos físicos
En nuestra entrada anterior, establecimos que las mezclas son uniones físicas de sustancias puras que no reaccionan químicamente. La gran ventaja de esto es que podemos separar sus componentes sin necesidad de complejas reacciones químicas, utilizando métodos sencillos basados en las propiedades físicas diferentes de cada componente.
A continuación, exploraremos algunos de los métodos de separación más comunes, clasificados según el tipo de mezcla.
1. Métodos para Separar Mezclas Heterogéneas
En las mezclas heterogéneas (donde se distinguen las fases, como agua y arena), aprovechamos las diferencias en tamaño de partícula o densidad.
A. Filtración
- Se utiliza para: Separar un sólido insoluble de un líquido (ejemplo: arena y agua).
- Principio: Se vierte la mezcla sobre un filtro (papel, tela, etc.). El líquido pasa a través de los poros del filtro, mientras que el sólido (residuo) queda retenido.

B. Decantación
- Se utiliza para: Separar un líquido menos denso de un líquido más denso (ejemplo: agua y aceite) o un sólido muy denso de un líquido (ejemplo: barro espeso).
- Principio: Se deja reposar la mezcla para que los componentes se separen por la acción de la gravedad. Luego, se vierte cuidadosamente la capa superior (o se usa un embudo de decantación) para separar las fases.

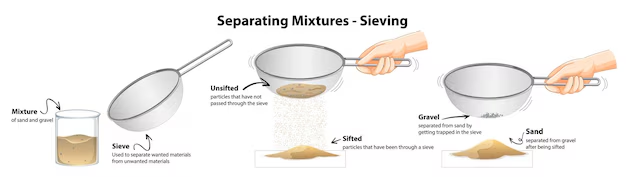
C. Tamización (o Cribado)
- Se utiliza para: Separar dos o más sólidos con diferente tamaño de partícula (ejemplo: harina y piedras pequeñas).
- Principio: Se pasa la mezcla a través de un tamiz o criba (una red con agujeros). Las partículas más pequeñas pasan, y las más grandes se retienen.
2. Métodos para Separar Mezclas Homogéneas (Disoluciones)
En las mezclas homogéneas o disoluciones (donde no se distinguen las fases, como agua con sal), los métodos suelen implicar un cambio de estado físico.
A. Evaporación y Cristalización
- Se utiliza para: Separar un sólido disuelto de un líquido (ejemplo: sal disuelta en agua).
- Principio: Se calienta la mezcla hasta que el componente líquido (disolvente) se evapora por completo, dejando el sólido (soluto) en el recipiente.
- Si el objetivo es obtener el sólido de forma pura, se llama cristalización. Si el objetivo es solo recuperar el líquido, se usa la destilación.

B. Destilación
- Se utiliza para: Separar dos líquidos miscibles (ejemplo: alcohol y agua) o un sólido disuelto de un líquido, recuperando ambos componentes.
- Principio: Se basa en la diferencia en los puntos de ebullición. La mezcla se calienta hasta que el líquido con el punto de ebullición más bajo se vaporiza primero. Este vapor se conduce a un condensador donde se enfría y vuelve a hacerse líquido (destilado), recogiéndose en otro recipiente.

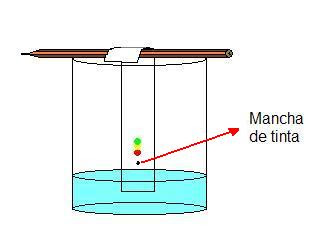
C. Cromatografía
- Se utiliza para: Separar componentes de mezclas complejas, a menudo líquidos o gases (ejemplo: analizar tintas de rotuladores).
- Principio: Se basa en la diferente velocidad con la que los componentes de la mezcla se desplazan a través de un medio fijo (como un papel o una columna) al ser arrastrados por un medio móvil (un líquido o gas).
Resumen Rápido
La elección del método de separación depende siempre de la diferencia de propiedades entre los componentes. Si tienen diferente densidad, usamos decantación; si tienen diferente punto de ebullición, usamos destilación.
Actividad Propuesta: Imagina que accidentalmente mezclas arroz con lentejas. ¿Qué método de separación físico, de los estudiados, usarías para separarlos?
Aquí te dejo algunos links para poder ampliar la información si lo deseas:
https://www.equiposylaboratorio.com/portal/articulo-ampliado/metodos-de-separacion-de-mezclas Entrada en una web donde explica algunos métodos
https://youtu.be/kxNL9ZoQqCY?si=3C645K10RUYiVUfF Video de unos 10 mins de duración que te servirá para comprender un poquito mejor este apartado.



 Anterior
Anterior 
